兆候と症状
多くの患者は、最初は痛みを訴えますが、その痛みは夜間に悪化する場合があり、断続的で、強さはさまざまで、しばらく続いている場合もあります。スポーツをする十代の若者は、大腿骨の下部または膝のすぐ下の痛みを訴えることがよくあります。腫瘍が大きい場合は、明らかな局所的な腫れとして現れることがあります。影響を受けた骨は正常な骨ほど強くなく、軽度の外傷で異常に折れる可能性があるため、突然の骨折が最初の症状となる場合があります。以下のような、皮膚にそれほど近くない深部腫瘍の場合: B. 骨盤領域では、局所的な腫れが見えない場合があります。

原因
いくつかの研究グループが、がん幹細胞とその腫瘍を引き起こす可能性、さまざまな表現型の原因となる遺伝子やタンパク質を研究しています。まれな原因として、関連のない病気に対する放射線療法が原因となる場合があります。
- 染色体 13q14 の欠失により網膜芽細胞腫遺伝子が不活化される家族性の症例は、骨肉腫を発症する高いリスクと関連しています。
- 骨パジェット病、線維性異形成、軟骨内腫症、遺伝性多発性外骨腫などの骨形成異常は、骨肉腫のリスクを高めます。
- リ・フラウメニ症候群(生殖系列変異 TP53) は、骨肉腫の発症の素因です。
- ロスムント・トムソン症候群(先天性骨欠損、毛髪および皮膚の異形成、 性腺機能低下症、および白内障の常染色体劣性遺伝)は、この疾患のリスク増加と関連しています。
- ボーンシーカーと呼ばれる原子炉からの高線量のストロンチウム90放出は、動物の骨がんや白血病のリスクを高め、人間でも同様であると疑われている。
そうではないことを示唆する根強い噂にもかかわらず、水のフッ素添加と癌または癌関連の死亡、つまり癌全般、特に骨癌と骨肉腫との間に明確な関連性はありません。多くの研究は、水中のフッ化物濃度が骨肉腫と関連することはないと結論付けています。フッ化物曝露と骨肉腫との関連性に関する考えは、雄ラットにおけるフッ化物と骨肉腫との関連性の不確かな証拠を示した 1990 年の米国国家毒物学プログラムの研究に由来しています。しかし、マウスにおけるフッ化物の発がん性の傾向を示す確かな証拠はまだありません。水のフッ素添加は、国民の歯の健康を改善するために世界中で実施されています。健康にも大成功だと考えられています。水道中のフッ化物の濃度は規制されており、米国環境保護庁はフッ化物濃度が 1 リットルあたり 4 ミリグラムを超えてはならないと規制しています。実際、水道にはすでに天然のフッ化物が含まれていますが、多くの地域社会では虫歯を減らすためにフッ化物をさらに添加することを選択しています。フッ化物は新しい骨の形成を引き起こすことも知られています。しかし、さらなる研究により、人間はフッ素添加水によって骨肉腫のリスクにさらされていないことが示されています。ほとんどの研究では、飲料水中にさまざまな濃度のフッ化物が存在する特定の地域での骨肉腫患者の数が数えられています。データの統計分析では、フッ素添加地域の違いによる骨肉腫症例の頻度に有意な差はないことが示されています。もう一つの重要な研究は、骨肉腫患者から骨サンプルを収集してフッ化物濃度を測定し、新たに診断された悪性骨腫瘍からの骨サンプルと比較することでした。その結果、骨肉腫患者と腫瘍対照から採取した骨サンプル中の平均フッ化物濃度には大きな差はありません。骨内のフッ化物濃度だけでなく、骨肉腫患者のフッ化物曝露量も健康な人と大きく変わらないことが証明されています。
機構
骨肉腫は骨成長部位で発生する傾向がありますが、これはおそらく、増殖によりこの領域の骨芽細胞が細胞形質転換を引き起こす可能性のある突然変異を受けやすくなるためと考えられます (RB 遺伝子と p53 遺伝子が関与することが多い)。この傾向のため、一部の大型犬種(セント・バーナードやグレート・デーン)では骨肉腫の発生が非常に一般的です。腫瘍は長骨の端(多くの場合骨幹端)に位置することがあります。ほとんどの場合、脛骨または上腕骨の近位端、または大腿骨の遠位端に影響を及ぼします。骨肉腫は、症例の 60% で膝の周囲の領域、15% で股関節、10% で肩、8% で顎に影響を及ぼします。石灰化した骨の腫瘍スパイクが直角に放射状に広がっているため、腫瘍は硬く、硬く、不規則な形をしています(X線検査で「クリスマスツリー」、「虫食い」、または「日焼け」のように見えます)。これらの直角は、コッドマンの三角形として知られるものを形成します。これは特徴的ですが、骨肉腫の診断にはなりません。周囲の組織が浸潤しています。顕微鏡: 骨肉腫の特徴は、腫瘍内に類骨 (骨形成) が存在することです。腫瘍細胞は非常に多形性 (未分化) であり、巨大で多数の非定型有糸分裂を伴うものもあります。これらの細胞は、中心石灰化(血酸親和性/青色、顆粒状)腫瘍骨の有無にかかわらず、不規則な小柱(無定形、好酸球性/ピンク色)を表す類骨体を生成します。腫瘍細胞は類骨基質に含まれています。存在する腫瘍細胞の特徴 (骨細胞、軟骨細胞、または線維芽細胞に似ているかどうか) に応じて、腫瘍を下位分類できます。骨肉腫には、多核の破骨細胞様巨細胞が存在する場合があります。
診断
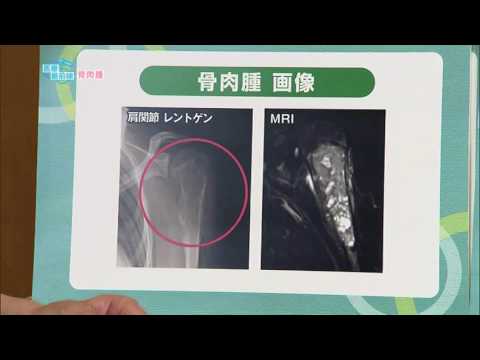
かかりつけ医や整形外科医が悪性の骨腫瘍を診ることはほとんどありません(ほとんどの骨腫瘍は良性です)。骨肉腫を診断する手順は通常、X 線検査で始まり、スキャン (CT、PET、骨スキャン、MRI) の組み合わせが続き、外科的生検で終わります。 X 線でよく見られる特徴の 1 つはコッドマン三角です。これは本質的に骨膜下病変であり、骨膜が腫瘍によって隆起したときに発生します。フィルムは示唆を与えますが、骨生検は腫瘍が悪性か良性かを判断する唯一の決定的な方法です。ほとんどの場合、骨肉腫の初期兆候は、定期的な歯科検査で撮影される X 線写真で捕らえられます。骨肉腫は下顎(下顎)に発生することがよくあります。したがって、歯科医は骨肉腫を示す可能性のある兆候を探すように訓練されています。この癌の X 線所見は広範囲に異なりますが、通常は歯根膜腔の対称的な拡大が見られます。歯科医が骨肉腫やその他の基礎疾患の存在を疑う理由がある場合、生検のために患者を口腔顎顔面外科医に紹介します。非顔面以外の骨肉腫の疑いがある場合の生検は、資格のある整形外科腫瘍医が実施する必要があります。米国癌協会は、「おそらく、この処置を適切に実施することがこれほど重要な種類の癌はないでしょう。生検が不適切に実施されると、患肢を切断から救うことが困難になる可能性があります。」と述べています。転移は肺にも転移する可能性があり、主に胸部 X 線検査で下部領域に単一または複数の丸い小結節として現れます。
バリエーション
- 従来型: 骨芽細胞、軟骨芽細胞、線維芽細胞の OS
- 毛細血管拡張性OS
- スモールセルOS
- 低品質の中央 OS
- 骨膜OS
- 傍骨OS
- セカンダリOS
- 高品質のサーフェス OS
- 骨格外OS
処理
骨肉腫の治療法としては、癌の完全根治的外科的一括切除が選択されます。約90%の患者は四肢切除手術を受けることができますが、合併症、特に感染症、プロテーゼの緩みと癒合不全、または局所的な腫瘍の再発により、さらなる手術や切断が必要になる場合があります。ミファムルチドは、手術後に腫瘍を除去するために使用され、化学療法と併用して、残っているがん細胞を死滅させてがんの再発リスクを軽減します。腫瘍切除後に回転形成術を行うことも可能です。骨肉腫患者の治療には、肉腫の治療経験のある腫瘍内科医および整形外科腫瘍医が最適です。現在の標準治療は術前化学療法(手術前の化学療法)とそれに続く外科的切除です。手術後に腫瘍内で見られる腫瘍細胞壊死(細胞死)のパーセンテージは、予後の見通しを与え、腫瘍学者に手術後に化学療法レジメンを変更する必要があるかどうかを知らせることにもなります。標準治療は、可能であれば四肢の整形外科手術(場合によっては切断)と、高用量メトトレキサートとロイコボリンレスキュー、動脈内シスプラチン、アドリアマイシン、イホスファミドとメスナ、BCD(ブレオマイシン、シクロホスファミド、ダクチノマイシン)、エトポシド、ムラミルトリペプチド。回転形成術を使用することができます。イホスファミドは、壊死率が低い場合の補助治療として使用できます。骨肉腫に対する化学療法は成功しているにもかかわらず、小児がんの生存率は最も低いものの 1 つです。報告されている最も良好な 10 年生存率は 92% です。使用されるプロトコールは、動脈造影反応に基づいて治療を個別化する積極的な動脈内療法です。いくつかの研究では、3 年の無イベント生存率は 50% ~ 75%、5 年生存率は 60% ~ 85+% です。全体として、5 年前に治療を受けた患者の 65 ~ 70% が現在も生存していることになります。これらの生存率は全体の平均であり、個々の壊死率によって大きく異なります。フィルグラスチムまたはペグフィルグラスチムは、白血球と好中球の数をカウントするのに役立ちます。輸血とエポエチン アルファは貧血に役立ちます。骨肉腫細胞株のパネルに対するコンピューター解析により、骨肉腫における新たな共通および特異的治療標的(プロテオーム的および遺伝的)が同定され、表現型からは腫瘍微小環境の役割の増加が示されました。

疫学
骨肉腫は、小児がんの中で 8 番目に一般的な形態です。これは、小児におけるすべての悪性腫瘍の 2.4%、およびすべての原発性骨がんの約 20% を占めます。 20歳未満の米国患者における骨肉腫の発生率は、一般人口では年間100万人あたり5.0人と推定されているが、黒人、ヒスパニック系、白人の間ではわずかな差がある(それぞれ100万人あたり6.8、6.5、4.6)。年間)。それは女性(年間100万人あたり4.0人)よりも男性(年間100万人あたり5.4人)の方がわずかに一般的です。より一般的には長骨の骨幹端領域に由来し、骨の 42% が女性、19% が脛骨、10% が上腕に発生します。全症例の約 8% が頭蓋骨と顎で発生し、さらに 8% が骨盤で発生します。米国では診断を受けた900人のうち約300人が毎年死亡している。発生率の 2 番目のピークは高齢者で発生し、通常は骨パジェット病などの基礎的な骨病変に関連しています。
予報
予測は 3 つのグループに分けられます。
- ステージ I の骨肉腫はまれで、傍骨骨肉腫または低悪性度の中心性骨肉腫が含まれます。広範囲切除の場合、予後は良好 (>90%) です。
- II期の予後は、腫瘍の位置(脛骨近位、大腿骨、骨盤など)、腫瘍塊のサイズ、および術前化学療法による壊死の程度によって異なります。 P 糖タンパク質のグレード、腫瘍が cxcr4 陽性か Her2 陽性かなどの他の病理学的要因も、肺への遠隔転移に関連するため重要です。転移性骨肉腫患者の予後は、転移までの期間が長く(12 か月以上から 4 か月)、転移の数が少なく、切除可能であるほど改善します。転移までの期間が長いよりも、転移が少ない方が良いのです。期間が長く(24 か月以上)、リンパ節の数が少ない(2 つ以下)場合は、転移後 2 年生存率が 50%、5 年生存率が 40%、10 年生存率が最も良好です。・年間生存率は20%。転移が局所的かつ局所的である場合、予後はより悪くなります。
- 肺転移を伴うステージ III の骨肉腫の最初の症状は、原発腫瘍と肺結節の切除可能性、原発腫瘍の壊死の程度、およびおそらく転移の数によって異なります。全生存予後は約 30% です。
小児がんによる死亡者数は不明ですが、骨や関節の悪性新生物による死亡が占めています。骨肉腫による死亡率は年間約 1.3% 減少しています。骨肉腫の長期生存確率は 20 世紀後半に劇的に改善し、2009 年には約 68% になりました。
動物
危険因子
骨肉腫は犬で最も一般的な骨腫瘍であり、通常、アイリッシュ・ウルフハウンド、グレイハウンド、ジャーマン・シェパード、ロットワイラー、山岳犬種(グレート・ピレニーズ、セント・バーナード、レオンバーガー、ニューファンドランド)、ドーベルマン・ピンシャー、グレートデーン。犬では人間よりも10倍多く発生します。セントバーナード犬では遺伝的根拠が示されています。避妊・去勢手術を受けた犬は、無傷の犬に比べて骨肉腫を発症する可能性が2倍高くなります。寄生虫 Spirocerca lupi の感染は、食道に骨肉腫を引き起こす可能性があります。
臨床症状
最も影響を受ける骨は、「肘から遠く、膝に近い」という基本前提に従い、上腕骨近位部、橈骨遠位部、大腿骨遠位部、および脛骨です。他の場所には、肋骨、下顎、脊椎、骨盤が含まれます。まれに、骨肉腫が軟組織から発生することがあります (骨格外骨肉腫)。手足の骨に影響を及ぼす腫瘍の転移は非常に一般的で、通常は肺に転移します。腫瘍は激しい痛みを引き起こし、影響を受けた骨の骨折につながることもあります。ヒトの骨肉腫と同様、骨生検は確定診断に至るための確実な方法です。骨肉腫は、他の骨腫瘍や骨髄炎などの他の多くの病変と区別する必要があります。頭蓋骨の骨肉腫の鑑別診断には、とりわけ、 軟骨肉腫および多葉骨腫瘍が含まれます。
治療と予後
切断が最初の治療法ですが、それだけでは転移を防ぐことはできません。切断と化学療法を組み合わせると生存率は向上しますが、それでもほとんどの犬は 1 年以内に死亡します。脚を救うことを目的とした外科的技術(四肢温存手術)では予後は改善されません。いくつかの最近の研究では、アレンドロネートやパミドロネートなどの破骨細胞阻害剤が骨溶解を軽減し、それによって痛みの程度や病的骨折のリスクを軽減することで生活の質にプラスの効果をもたらす可能性があることが示唆されています。
猫
骨肉腫は、それほど一般的ではありませんが、猫で最も一般的な骨腫瘍でもあり、主に後肢に影響を与えます。一般に猫のがんは犬よりも進行性が低いため、切断だけでも多くの罹患猫は生存率が高くなりますが、組織病理学的に高悪性度が確認された場合には切断後に化学療法が推奨されます。
- ネバダ州コシキナ。コーリー、S (2008)。 「骨肉腫の肺転移を治療するための新規標的」。エスン。 2009 年 4 月 14 日に取得。
- ウィズロウ、S.J. (2003)。 「四肢温存試験と犬の骨肉腫」。遺伝子、犬、がん: 第 3 回犬がんカンファレンス、2003 年。 2006 年 6 月 16 日に取得。
- Loukopoulos P、ソーントン JR、ロビンソン WF (2003 年 5 月)。 「犬の骨腫瘍におけるp53インデックスの臨床的および病理学的関連性」。獣医病理学。 40 (3): 237–48。土井:10.1354/vp.40-3-237。 PMID 12724563。
- ルー、B.テッラチーニ、G.他。 (1998年)。 「犬の骨肉腫の宿主関連危険因子」。獣医 J. 156 (1): 31-9。土井:10.1016/S1090-0233(98)80059-2。 PMID 9691849。
- サイカス、V。ルコポロス、P;ポリゾポウロウ、ZS。ソフィアニディス、G (2009 年 3 月)。 「犬の重度の脳および小脳圧迫を引き起こす尾側頭蓋の多葉性腫瘍」。獣医学ジャーナル。 10 (1):81–3。土井:10.4142/jvs.2009.10.1.81。 PMC 2801101。 PMID 19255529。
- ゲルバーグ KH、フィッツジェラルド EF、ファン SA、ダブロウ R (1995 年 12 月)。 「フッ化物曝露と小児骨肉腫:症例対照研究」。アメリカ公衆衛生ジャーナル。 85 (12): 1678–83。土井:10.2105/AJPH.85.12.1678。 PMC 1615731。 PMID 7503344。
- Bech-Nielsen S、Haskins ME、他。 (1978年)。 「セント・バーナード犬の第一度近親者における骨肉腫の頻度」。国立がん研究所60 (2): 349–53。土井:10.1093/jnci/60.2.349。 PMID 271748。
- マホニー MC、ナスカ PC、バーネット WS、メリウス JM (1991 年 4 月)。 「ニューヨーク州の骨がん発生率:時間的傾向とフッ素添加飲料水」。アメリカ公衆衛生ジャーナル。 81 (4): 475–9。土井:10.2105/AJPH.81.4.475。 PMC 1405037。 PMID 2003628。
- オスナ D、デ アラバ E (2009)。 「肉腫の分子病理学」。最近の臨床試験の改訂。 4 (1): 12-26。土井:10.2174/157488709787047585。 PMID 19149759。
- 「Sr-90 は動物の骨がんや白血病のリスクを高めることが知られており、人間でも同様であると推定されています。グーグル(原子炉はストロンチウムを放出する)の結果 2 より」。
- 「フッ化物」、オーストラリア政府国家健康医学研究評議会。
- ブッカー PJ、ゲブハルト M、ウェーバー K (2005)。 「骨肉腫」。エスン。 2009 年 4 月 15 日に取得。
- Ranen E、Lavy E、Aizenberg I、Perl S、Harrus S (2004)。 「スピロセルコーシスに関連した犬の食道肉腫。17 例の後ろ向き研究 (1997 ~ 2003 年)」。獣医寄生虫学。 119 (2-3): 209-221。土井:10.1016/j.vetpar.2003.10.023。 PMID 14746980。
- パパラス JA、バルマー NN、ウォレス C、サングエザ OP (2009 年 6 月)。 「破骨細胞様巨細胞を伴う骨化性皮膚線維腫:症例報告と文献レビュー」。 J デルマトパトールです。 31 (4): 379–83。土井:10.1097/DAD.0b013e3181966747。 PMID 19461244。
- 「がんの神話: フッ素とがん」西オーストラリア州がん評議会。
