プレゼンテーション
ユーイング肉腫は男性に多く(男性 1.6 人:女性 1 人)、通常は小児期または成人期初期に発生し、ピークは 10 ~ 20 歳です。それは体のどこにでも発生する可能性がありますが、骨盤および近位長骨、特に成長板の領域で最も一般的です。大腿骨の骨幹が最も一般的な部位であり、脛骨、上腕骨がそれに続きます。 30%は発症時に明らかに転移性である。患者は通常、極度の骨の痛みに悩まされます。まれに、膣内で発症することもあります。兆候と症状には、間欠的な発熱、 貧血、白血球増加、沈降速度の増加、および全身性炎症疾患のその他の症状が含まれます。腫瘍の種類、進行度、位置によっては、激しい痛みが発生する場合もあります。 Bone Cancer Research Trust (BCRT) によると、最も一般的な症状は、局所的な痛み、腫れ、さまざまな強さの散発的な骨の痛みです。肉腫が体の表面近くの骨にある場合、腫れは目で確認できる可能性が最も高くなりますが、骨盤など、体のより深い他の場所で発生した場合は見えない場合があります。
原因
染色体間の遺伝子交換により、細胞が癌化する可能性があります。 ユーイング肉腫のほとんどの症例 (85%) は、染色体 11 と染色体 22 の間の転座の結果であり、染色体 22 の EWS 遺伝子が染色体 11 の FLI1 遺伝子と融合します。 EWS/FLI はメインレギュレーターとして機能します。他の転座は t(21;22) と t(7;22) にあります。ユーイング肉腫細胞は、CD99 および MIC2 に対して陽性であり、CD45 に対して陰性です。
診断
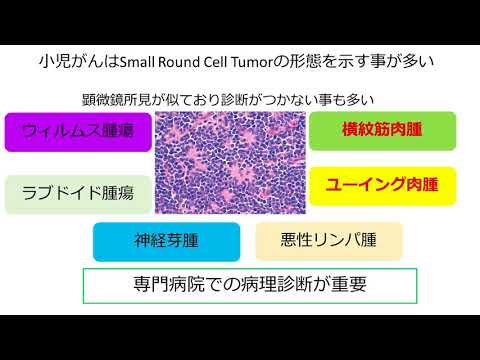
最終的な診断は、組織形態学的所見、免疫組織化学および分子病理学に基づいて行われます。ユーイング肉腫は小さな青色の丸い細胞腫瘍で、通常、グリコーゲンにより H&E 染色で透明な細胞質が見られます。グリコーゲンの存在は、PAS 染色陽性および PAS ジアスターゼ染色陰性によって証明できます。特徴的な免疫染色は CD99 で、細胞膜を拡散的に標識します。形態学的および免疫組織化学的所見は、関連する染色体転座によって確認され、そのうちのいくつかが発生します。ユーイング肉腫症例の約 90% で発生する最も一般的な転座は t(11;22)(q24;q12) で、これはEWSR1 遺伝子とFLI1 遺伝子を融合することによって異常な転写因子を作成します。病理学的鑑別診断は、リンパ腫、肺胞横紋筋肉腫、線維形成性小円形細胞腫瘍などの青色の小さな円形細胞腫瘍をグループ化することです。

鑑別診断
同様の臨床症状を示す他の疾患には、 骨髄炎、 骨肉腫(特に毛細血管拡張性骨肉腫)、および好酸球性肉芽腫が含まれます。隣接する骨に浸食する多形性未分化肉腫 (悪性線維性組織球腫) などの軟部組織新生物も、同様の外観を示すことがあります。
画像処理手順
従来の X 線写真では、最も一般的な骨の外観は、骨膜反応を伴う浸透性溶解性病変です。層状または「タマネギの皮」様の骨膜反応の古典的な説明は、この病変に関連付けられることがよくあります。滑らかなフィルムは、最初の検査またはスクリーニング中に貴重な情報を追加します。広い移行ゾーン(例えば、透過性)は、良性の病変を進行性または悪性の溶解性病変から区別する際に、滑らかなフィルムの最も有用な特徴である。悪性腫瘍の診断には磁気共鳴画像法 (MRI) を日常的に使用する必要があります。これは、骨組織と軟組織の全範囲を示し、腫瘍を近くの他の解剖学的構造(血管など)と関連付けます。ガドリニウム造影は、非造影研究に比べて追加情報が得られないため必要ではありませんが、一部の現在の研究者は、動的造影MRIが腫瘍内の壊死の範囲を決定し、手術治療に対する反応を予測するのに役立つ可能性があると主張しています。軸方向コンピュータ断層撮影 (CT) は、特に頭蓋骨、脊椎、肋骨、骨盤における腫瘍の骨外への広がりを調べるために使用することもできます。 CT と MRI は両方とも、放射線および/または化学療法に対する反応を監視するために使用できます。骨シンチグラフィーは、治療に対する腫瘍の反応を追跡するために使用することもできます。ユーイング肉腫、骨リンパ腫、および小細胞骨肉腫を含む悪性小細胞円形腫瘍のグループでは、ハバース管で浸透性増殖が起こる一方で、皮質は X 線写真ではほぼ正常に見えることがあります。これらの腫瘍には大きな軟組織塊が伴う場合がありますが、骨破壊はほとんど見られません。 X線検査では、皮質破壊の兆候が見られないことがよくあります。 X線撮影では、ユーイング肉腫は延髄の「虫食い」の破壊的な透視像と拡大を伴う皮質の侵食として現れます。
処理
ほぼすべての患者は、多剤化学療法(多くの場合、イホスファミドとエトポシドを含む)と、手術および/または放射線による局所疾患管理を必要とします。一見局所的な疾患を持つ患者のほとんどすべてが、診断時に実際には無症候性の転移性疾患を抱えているため、積極的なアプローチが必要です。治療は多くの場合、ビンクリスチン、ドキソルビシン、シクロホスファミドとイホスファミドおよびエトポシドを含む術前化学療法で行われます。約 3 か月の化学療法の後、残った腫瘍は外科的に切除されるか放射線照射、またはその両方が行われます。外科的切除には、四肢の救済または切断が含まれる場合があります。検査時に悪性腫瘍が確認された場合、生検時に完全切除が行われる場合があります。治療期間は診断時の病気の部位と段階によって異なります。根治的化学療法は 3 週間のサイクルで最大 6 回の治療を受けることができますが、ほとんどの患者は化学療法を 6 ~ 12 か月、放射線療法を 5 ~ 8 週間受けます。局所的な疾患には放射線療法が使用されました。この腫瘍は放射線に非常に敏感であるという独特の特性を持っており、これは「雪のように溶ける」という表現で認識されることもありますが、主な欠点は、しばらくすると劇的に再発することです。 EWS-ETS遺伝子転座に続発するユーイング肉腫の発症に関連する発癌性融合タンパク質の発現を下方制御するアンチセンスオリゴデオキシヌクレオチドが、可能な治療法として示唆されている。さらに、合成レチノイド誘導体フェンレチニド (4-ヒドロキシ(フェニル)レチンアミド) は、in vitroでユーイング肉腫細胞株において高レベルの細胞死を誘導し、 in vivo マウスモデルにおいて異種移植片の増殖を遅らせることが報告されています。 2014年、LadraとYockは小児肉腫に対する陽子線治療に関する詳細な報告書を発表しました。彼らは、 横紋筋肉腫、非横紋筋肉腫軟部肉腫、骨肉腫、ユーイング肉腫、 脊索腫、 軟骨肉腫に対するさまざまな陽子線治療陽子線センターからの臨床データと線量測定データの両方を検討しました。彼らは、ほとんどの小児がん、肉腫、またはその他のカテゴリーにおいて、陽子線照射が優れた線量測定特性、特に積分線量の低減とリスク臓器への線量の低減をもたらすことを示唆する十分なデータがあると結論付けた。陽子線治療の線量測定上の優位性に起因することに加えて、陽子線および軟部肉腫に関する初期の臨床データは、歴史的な光子線対照と比較して転帰の同等または改善を示しているようであり、毒性も軽減される可能性があると指摘した。
妊孕性の温存
女性の場合、化学療法は卵巣を損傷し、 不妊症を引き起こす可能性があります。将来の妊娠から利益を得るために、女性は化学療法を開始する前に卵子または卵巣組織の凍結保存を行うことができます。ただし、後者は卵巣組織の再移植後に癌を再播種する可能性があります。実施する場合は、凍結保存した組織の移植前に、病理学的レベルと分子レベルの両方で卵巣組織の悪性腫瘍の痕跡を検査する必要があります。

予報
病期分類では、限局性疾患の患者と転移性疾患の患者を区別する試みが行われます。転移は最も一般的に乳房、骨、および/または骨髄で発生します。あまり一般的ではない部位には、中枢神経系やリンパ節などがあります。化学療法で治療した場合の局所疾患の 5 年生存率は 70% ~ 80% です。多剤化学療法を使用する前は、長期生存率は 10% 未満でした。化学療法、放射線、手術を含む集学的治療の開発により、現在の長期生存率はほとんどの臨床センターで 50% 以上に増加しています。ただし、一部の情報源では、25 ~ 30% であると述べています。 Idriss M. Bennani-Baiti (がんエピジェネティクス協会) が主導した遡及的患者研究では、2 つのケモカイン受容体 CXCR4 と CXCR7 が分子予後因子として使用できることが示されました。両方のケモカイン受容体の発現レベルが低い患者は長期生存の可能性が最も高く、診断後 5 年後の生存率が 90% 以上であるのに対し、両方の受容体の発現レベルが非常に高い患者では 5 年後の生存率が 30% 未満です。
疫学
ユーイング肉腫は原発性骨肉腫の 16% を占めます。米国では、最も一般的には人生の 20 年間に発生し、その発生率は 3 歳未満の小児では 100 万人あたり 0.3 人、15 ~ 19 歳の青少年では 100 万人あたり最大 4.6 人です。国際的には、年間発生率は平均して子供100万人当たり2件未満です。英国では、毎年平均 6 人の子供が診断を受けており、そのほとんどが思春期初期の男性です。 10代で診断されることが多いため、思春期の発症とこの病気の初期段階との間に関連性がある可能性がありますが、この仮説を支持する研究はありません。診断された既知の最高齢患者は76歳で、ニュージャージー州マーサー郡在住でした。ノースカロライナ州ウェイクフォレストに住む3人の血縁関係のないティーンエイジャーのグループがユーイング肉腫と診断された。 3人の子供たちは全員2011年に診断され、学校が改修されている間、全員が同じ仮設教室に一緒に通っていました。近くに住む4人目の10代の若者は2009年に診断された。このグループの可能性は大きいと考えられます。ユーイング肉腫はヒト集団における発生率に顕著な差があり、アフリカ人よりもヨーロッパ系の集団で約 10 ~ 20 倍多く発生します。ヨーロッパのユーイング肉腫患者数百人および遺伝的に一致する健康な対照者を対象に実施されたゲノムワイド関連研究(GWAS)では、染色体 1、10、および 15 上の 3 つの感受性遺伝子座が一貫して特定されました。追跡調査では、ユーイング肉腫であることが判明しました。感受性遺伝子 EGR2 は、染色体 10 の感受性遺伝子座内に位置し、GGAA マイクロサテライトを介してEWSR1-FLI1 融合癌遺伝子によって制御されます。ユーイング肉腫は、小児および青少年に 2 番目に多い骨がんであり、初回診断の約 70%、再発の 10 ~ 15% で予後および転帰が不良です。
研究、情報、サポート
英国とアイルランドでは、骨がん研究トラストが研究に資金を提供し、ユーイング肉腫やその他の骨がんに関する情報を提供しています。これには、この症状に苦しむ十代の若者向けの情報も含まれています。関連する副作用のない天然分子であるメラトニンは、ユーイング肉腫細胞株である SK-N-MC 細胞において細胞毒性を誘発することが以前に示されています。

- Turc-Carel C、Aurias A、Mugneret F、他。 (1988年6月)。 「ユーイング肉腫の染色体。I. t(11;22)(q24;q12) の顕著な一貫性を示す 85 例の評価」。がんジュネット。サイトジネット。 32 (2): 229–38。土井:10.1016/0165-4608(88)90285-3。 PMID 3163261。
- ローブ、デビッド M;モニカ・トゥワルツィオク。クラインシモン、スーザン。ヤナ・ロルフ。ハンター、セバスチャン。エガート、アンジェリカ。ジョージ・サイフェルト。デレビンスキー、カタリーナ I. (2016)。 「Viscum アルバム L の複数の活性化合物。相乗的に収束してユーイング肉腫のアポトーシスを促進」。プロスワン。 11 (9): e0159749。土井:10.1371/journal.pone.0159749。 ISSN 1932-6203。
- Jeon IS、Davis JN、Braun BS 他(1995年3月)。 「変異型ユーイング肉腫転座 (7;22) は、EWS 遺伝子を ETS 遺伝子 ETV1 に融合します。」がん遺伝子。 10 (6): 1229–34。 PMID 7700648。
- マテオ・ロサーノ S、ゴーカレ PC、ソルジャースコフ VA、ドリチロ A、ティラード OM、ノターリオ V (2006 年 11 月)。 「ユーイング肉腫におけるEWS/FLI-1の転写および翻訳ターゲティングの組み合わせ」。クリン。がん研究所12 (22): 6781–90。土井:10.1158/1078-0432.CCR-06-0609。 PMID 17121899。
- 「ACS :: ユーイング家系腫瘍はどのように進行するのか?」 2008年4月22日のオリジナルからアーカイブ。
- 「陽子線治療による小児腫瘍の治療の現在の実践、機会、課題」。 2015 年 10 月。|title= の 26 番目の位置にある改行文字 (ヘルプ)
- ランドール、R.L. (2005)。 「ユーイング肉腫ファミリーの腫瘍(ESFT)」。エスン。 2009 年 4 月 15 日に取得。
- カサド=ザピコ、サラ、他「ヒトユーイング肉腫癌細胞に対するメラトニンといくつかの化学療法薬の相乗的抗腫瘍効果: 外因性アポトーシス経路の増強」松果体研究ジャーナル 48.1 (2010): 72-80。学術検索プレミア。ウェブ。 2016 年 11 月 5 日。
- ポステル・ヴィネ、ソフィー。ベロン、アメリ S;フランク・ティロード。ピエロン、ガエル。ステファニー・レイノー。コヴァール、ハインリヒ。オベリン、オディール。ラプーブル、イブ。バレエ、ステリー。 「TARDBPおよびEGR2付近の一般的な変異は、ユーイング肉腫に対する感受性と関連している。」自然遺伝学。 44 (3): 323–327。土井:10.1038/ng.1085。 PMID 22327514。
- ウォーチ、ジェニファー。サイラス、ジョビン。ロバート、ゴールズビー。マッセイ、キャサリン K.ノイハウス、ジョン。デュボア、スティーブン G. (2011-03-01)。 「EWSR1転座に関連する間葉系腫瘍の発生率における人種差」。がん疫学バイオマーカーと予防。 20 (3): 449–453。土井:10.1158/1055-9965.EPI-10-1170。 ISSN 1055-9965。 PMC 3051020。 PMID 21212061。
- eMedicine でのユーイング肉腫画像処理
- 「軟部組織腫瘍: ユーイング腫瘍/原始神経外胚葉腫瘍 (PNET)」。腫瘍学および血液学における遺伝学および細胞遺伝学のアトラス。 2012 年 10 月 29 日のオリジナルからアーカイブ。2012 年 11 月 5 日に閲覧。
- マクティアナン AM、カッソーニ AM、ドライバー D、ミケラニョーリ MP、キルビー AM、ウィーラン JS (2006)。 「ユーイング肉腫再発後の転帰の改善: 単一施設からの 114 人の患者の分析」。肉腫。 2006 : 83548.doi:10.1155/SRCM/2006/83548。 PMC 1698143。 PMID 17496997。
- バーンスタイン M、コバール H、パウルッセン M、他。 (2006 年 5 月)。 「ユーイング肉腫ファミリーの腫瘍:現在の管理」。腫瘍学者。 11 (5): 503–19。土井:10.1634/theoncologist.11-5-503。 PMID 16720851。
- 「膣の腫瘍; 第 6 章」 (PDF)。国際がん研究機関、世界保健機関。 291–311ページ。
